樂活小編
在美國,約有600萬人患有阿茲海默症。這種疾病逐漸損害患者的記憶力和思考能力,最終使他們無法執行最簡單的任務。大多數阿茲海默症患者在進入老年後開始出現症狀。
雖然現在有一些藥物可以治療,但是由於價格昂貴,很少有人能够承受。
 聯邦健保計劃近日一份聲明稱,Medicare和Medicaid服務中心(CMS)將為患者使用阿茲海默症新藥Leqembi提供報銷,不過,這需要患者的醫生參與一項收集患者信息的登記活動。
聯邦健保計劃近日一份聲明稱,Medicare和Medicaid服務中心(CMS)將為患者使用阿茲海默症新藥Leqembi提供報銷,不過,這需要患者的醫生參與一項收集患者信息的登記活動。
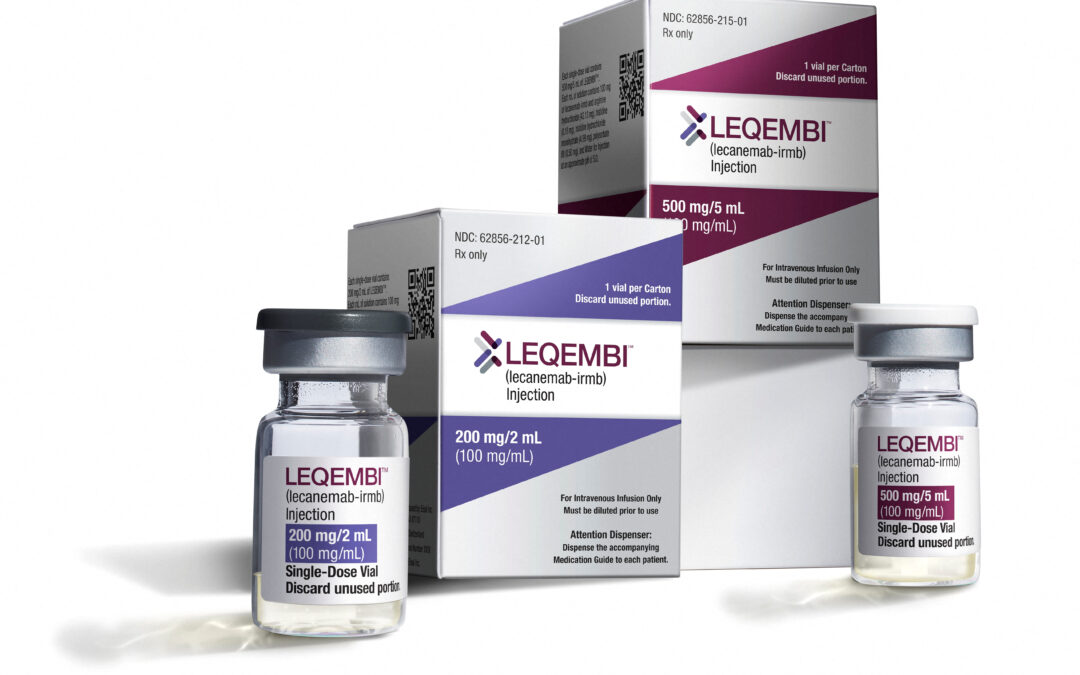
Leqembi是由日本公司衛材株式會社(Eisai Co.)和美國百健(Biogen Inc., BIIB)共同開發的一款新型阿兹海默症藥物,已於今年1月獲得食品和藥品管理局(FDA)的加速批准,並預計將在7月6日前獲得常規批准。
路透社稱,如果Leqembi獲得FDA的常規批准,它將成為首個“疾病修復”(disease-modifying)藥物。根據阿兹海默症協會的數據,目前的治療方法只能緩解症狀,但不能改變疾病的進程。
然而,這款新藥的價格設定為每年26,500美元,通過靜脈注射給藥,對年長者來說價格高昂。另外,專家提醒,該藥物可能存在副作用,包括腦腫脹或出血。
新的計劃要求阿兹海默症患者的醫生參與一項數據收集工作,即對患者進行登記,並由CMS對數據進行統一管理。
近日發布的情况說明書中提到,患者登記將在全美範圍内進行,可以通過CMS網站完成,登記信息將被免費使用。
為了獲得報銷,患者需被診斷為由阿兹海默症引發的輕度認知障礙或早期失智,並由一名合格的醫生進行登記。
醫生需要提交患者的人口統計信息、診斷信息,以及患者是否正在服用任何治療或預防血栓的藥物,因為這些藥物可能增加治療相關的腦出血風險。
CMS還希望收集該藥副作用的數據和評估患者狀况的認知測試信息。此外,醫生也需要提交腦部掃描、脊髓液測試或其他評估澱粉樣蛋白水平的檢測結果。澱粉樣蛋白是阿兹海默症的標誌性蛋白,Leqembi藥物和其他此類藥物的治療標靶。
去年11月發布的一項研究顯示,使用Leqembi的阿兹海默症早期患者的認知能力下降速度降低了27%,但也存在嚴重的副作用,如腦腫脹和出血或微出血。Leqembi在1月份獲得FDA加速批准後,CMS表示,只有在患者參加臨床試驗的情况下,才會為該藥提供報銷。
但患者權益倡導者擔心,新的登記要求可能將限制患者獲得這種藥物。
·50歲以上都在關注的公眾號·

樂活50加YouTube频道上線

訂閱+點讚+開啟小鈴鐺
是對樂活50加
最大的支持和鼓勵